2人の日本人研究者が挑む「ナノマシン」と「がん光免疫療法」
2018年03月20日
日本人研究者が開発した2つの革新的ながん治療法が、実用化に向けた臨床試験に進んでいる。高分子化学を駆使した「ナノマシン」と、がん細胞に光を当てて物理的に破壊する「がん光免疫療法」である。ともに専門分野を超えた好奇心が、既存の概念を覆すアイデアを生み出した。
 ナノマシンの仕組み図=ナノ医療イノベーションセンターのHPより
ナノマシンの仕組み図=ナノ医療イノベーションセンターのHPより「ナノマシン」は極小の高分子粒子の中に抗がん剤などの薬剤を包み込んだもの(図参照)。注射で体内に入れると、血流に乗って全身をめぐる。病院と同じように自動で検査や診断をし、患部で薬剤を放出して病気を治す。その働きから「体内病院」(In Body Hospital)とも呼ばれる。
 ナノ医療イノベーションセンターの片岡一則センター長兼研究統括(東京大学名誉教授)
ナノ医療イノベーションセンターの片岡一則センター長兼研究統括(東京大学名誉教授)1960年代のSF映画「ミクロの決死圏」では、人間が細菌サイズに小さくなって体内に入り病気を治療したが、そのシーンを彷彿(ほうふつ)とさせる。
主導するのは、川崎市産業振興財団のナノ医療イノベーションセンターの片岡一則センター長兼研究統括(東京大学名誉教授)=写真。元々は大学で合成化学を学んだ化学者である。
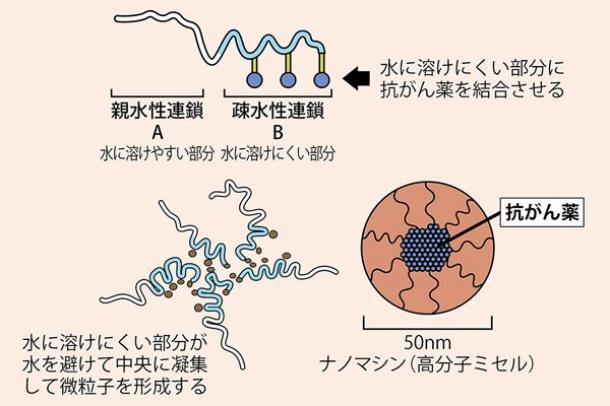
ナノマシンは図のように、水に溶けやすい性質(親水性)と、溶けにくい性質(疎水性)の両方を持った高分子を水の中に入れて作る。
高分子は親水性の部分を外側に、疎水性の部分を内側にして丸く凝縮するので、疎水性の部分にあらかじめ薬剤を付けておくと、薬剤を内包したナノマシンができる。
その適用が最も有望視され、臨床試験が行われているのが、がん治療である。
ナノマシンの大きさはウイルスと同程度の直径約50ナノメートル(1ミリの2万分の1)ある。正常な組織では血管壁の穴が小さくて血管の外へ出られないが、がん組織は大量の栄養や酸素を必要とするので穴が100ナノメートルと大きく、ナノマシンは容易にがんの中に入っていける。
がん組織は酸性になるので、ナノマシンはそれを検知すると自ら壊れ、抗がん剤を一気に放出するよう設計されている。
臨床試験は5種類のがんを対象に行われており、中でも乳がんとすい臓がんは、安全性を見るフェーズ1、効果の有無を調べるフェーズ2を終え、今は最終のフェーズ3(他の治療法との比較)に入っている。
ナノマシンは、従来のがんの外科手術や薬物治療、放射線治療とは全く異なるメカニズムで機能する。片岡氏は生体材料(バイオマテリアル)を研究するうちに、高分子粒子をがん治療に応用する発想を得た。
有料会員の方はログインページに進み、デジタル版のIDとパスワードでログインしてください
一部の記事は有料会員以外の方もログインせずに全文を閲覧できます。
ご利用方法はアーカイブトップでご確認ください
朝日新聞社の言論サイトRe:Ron(リロン)もご覧ください