時代を画する新薬誕生だが、期待しすぎてはいけないこれだけの理由
2021年06月10日
不治と言われてきたアルツハイマー病が治るようになるのか、と期待した人は多いだろう。が、事はそう簡単ではない。これは初期段階、つまり「まだあまり困っていない段階」に使う薬である。認知機能が明らかに衰えたアルツハイマー病患者は対象ではない。
果たしてあまり困っていないときに薬を使う気になるだろうか。しかも高価と来ている。医療経済からはどう評価すべきなのだろう。そもそも、早め早めの検査は望ましいことなのだろうか。悩みを増やすだけにならないのだろうか。
確かに、比較的若い時期に発症する家族性アルツハイマー病にとっては、待望の治療薬である。これで救われる患者が出れば、史上初の画期的な出来事になる。しかし、一般的なアルツハイマー病にとってどうなのか。むしろ、社会は新たな難題をつきつけられたのではないか。
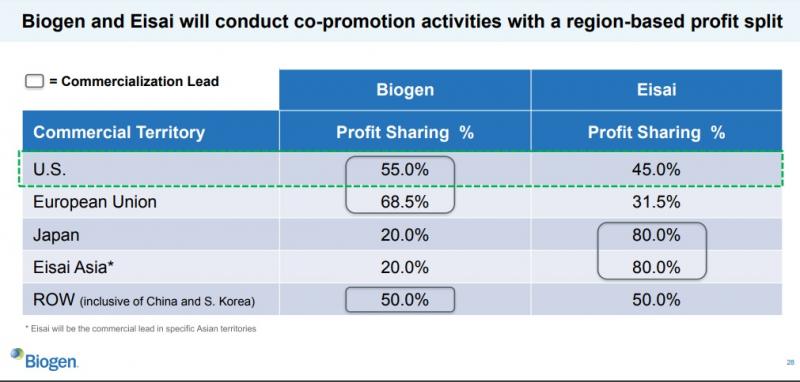 米バイオジェンとエーザイの共同開発の内容=米バイオジェン社のホームページから
米バイオジェンとエーザイの共同開発の内容=米バイオジェン社のホームページから アルツハイマー治療薬「アデュカヌマブ」=米バイオジェン社提供
アルツハイマー治療薬「アデュカヌマブ」=米バイオジェン社提供アデュカヌマブも臨床試験の結果をめぐって判断が揺れ、第三相試験(承認申請に必要な最後の試験)の最中にバイオジェン社は開発中止をいったん決めた。ところがデータを精査すると、薬の量が多いほど、また期間が長いほどアミロイドβを減らす効果が出ていた。さらに、金銭管理や家事などの日常生活の評価でも効果が見られ、一転して承認申請することに。
FDAは2020年に優先審査を決定した。ところが、FDAが招いた外部委員による諮問委員会では「エビデンスが不十分」という意見が大勢を占めて、早期承認は頓挫。追加データを解析するため審査期限が延長され、こうして6月7日に「今後、臨床的有用性を確認する対照試験をする」という条件つきで承認されたのである。
エーザイは認知症の進行を抑制する「アリセプト」(1999年に承認)を開発した会社である。この薬は神経の働きを活発にさせることで、進行を遅らせる。つまり、対症療法としての薬である。そうではなく、アルツハイマー病の原因に働きかける「根本治療薬」を生み出したいーーこれはエーザイに限らず世界中の製薬企業と研究者の、さらに言えば患者の夢だった。
ところが、問題があった。
有料会員の方はログインページに進み、デジタル版のIDとパスワードでログインしてください
一部の記事は有料会員以外の方もログインせずに全文を閲覧できます。
ご利用方法はアーカイブトップでご確認ください
朝日新聞社の言論サイトRe:Ron(リロン)もご覧ください