2012年02月17日
==============================================
朝日グループのジャーナリズムTV「朝日ニュースター」は、通信衛星などを利用して24時間放送しているテレビチャンネルで、ケーブルテレビ局やスカパー!などを通じて有料視聴することができます。昨年4月から始まった「科学朝日」は、高橋真理子・朝日新聞編集委員がレギュラー出演する科学トーク番組です。WEBRONZAでは、番組内容をスペシャル記事としてテキスト化してお届けします。
====================================================================

ゲスト:理化学研究所発生・再生科学総合研究センター細胞分化・器官発生グループリーダー 笹井芳樹さん
高橋:こんばんは。科学の最先端にひたる『科学朝日』。案内役の高橋真理子です。本日取り上げるテーマは「発生生物学から再生医療へ」です。発生生物学というのは、一つの卵がどんどん細胞分裂を繰り返して赤ちゃんができていくという、生物の不思議のなかでももっとも不思議な部分を解明する学問です。その基礎研究から新しい治療法が生まれようとしています。駄目になった組織を作り直すというという、再生医療です。本日は、目の奥にある網膜を、ネズミの細胞を使ってではありますけれども、世界で初めて人工的に作り出した、理化学研究所発生・再生科学総合研究センター細胞分化・器官発生グループ、グループディレクターの笹井芳樹(ささい・よしき)さんをゲストにお迎えしました。こんばんは。よろしくお願いいたします。
笹井:こんばんは。よろしくお願いいたします。
高橋:さっそくですけれども、先日ですね、胚性幹細胞、いわゆるES細胞を使って黄班変性、これ、年とった方にはかなり多い病気だと伺ってますけれども。
笹井:そうですね。
高橋:その患者さんに網膜の組織を移植して、視力の回復が見られたというニュースがございました。これは世界で初めてのことなんでしょうか。
笹井:そうですね。ES細胞は、ヒトのES細胞としては13年から14年ほど前にアメリカで作られて、それ以来、ヒトにこうして移植して、難病を治そうという研究が進んできたわけですけども、そのなかでも網膜というのは、非常に皆さん興味がある、非常に期待している領域なんです。世界で今いくつか、数箇所ぐらいの研究機関がしのぎを削って網膜の治療をやっています。そのなかの一つの試みとして、アメリカのベンチャー企業が、網膜の中で1種類の、ある細胞、それを移植したというふうな例になります。
高橋:アメリカではベンチャー企業がやってるんですね?
笹井:そうですね。ベンチャー企業とアメリカの大学が提携してやっているわけなんですが、今回のものは網膜の中でも、網膜そのものというよりも、網膜の外側に網膜をくるむように存在している色素上皮という細胞の移植で、これは網膜を保護する役割があります。この細胞が、年をとったり、あるいは遺伝的な理由で機能しなくなってくると、網膜自体も傷んできますので、それをES細胞から作った細胞で移植して交換しようと、そういうふうな試みのものです。
高橋:なるほど。黄班変性という病気は、網膜の中でも一番上の部分の膜が傷んでくる病気ということなんですね。
笹井:そうですね。特に年をとって出てくる、加齢黄班変性という病気については、かなり多い病気で、日本でも数万人の患者さんがそのせいで視力を大きく落としている。そこまで行かない、軽い例で言うと、その何倍かもあるというふうに言われている病気です。ただ、今回の治療については、実は世界中で、先ほども申しましたように、激しい開発競争になっているんですが、まだやりだしたところです。2例の患者さんに対して移植してみたら、まずは悪い効果はなかった、と。副作用はなかった。それで少し視力が改善したのではないか、というのを示唆するデータが出てきたというところで、今後もう少し詳しい研究、それからフォローアップをする必要があります。
高橋:なるほど。視力が劇的に回復したとまでは言えないわけですね。
笹井:そうですね。まだフォローアップの期間も短いですし、もう少したくさんの例、そしてたくさんの違ったアプローチでの研究が進もうとしていますので、それらを総合してどのぐらい治療効果があるのかということを見る必要があるのですが、私たちは非常にこれについては期待して、新しい治療法になるのではないかと思っています。
高橋:なるほど、なるほど。で、先生がお作りになったのは、上皮、一番上のところだけじゃなくて、網膜全体ということなんですね?
笹井:そうですね。私たちのところでも、この網膜の一番外側にある色素上皮をES細胞やiPS細胞から作って、それを移植しようという研究を、神戸の私たちの研究所と病院とでやっているのですけども、その部分というのは、網膜を保護する作用はあるんですが、光を見る部分ではないわけなんですね。光を感じる、そして脳に伝える部分、これが網膜の中心的な部分なんですが、そこの部分を今回はES細胞から作ることができたということになります。
高橋:ふーん。そうすると今度はそこの部分が病気の方の治療に道を開くということになりますね。
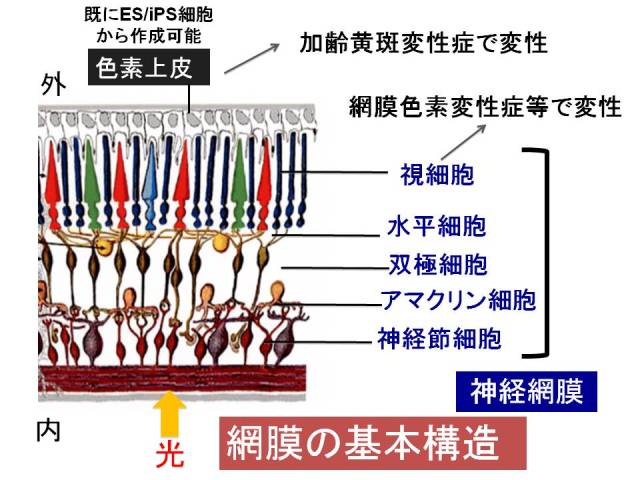
笹井:そうですね。実はこの光を受けて脳に伝える部分、「神経網膜」と言いますが、ここには6種類の細胞があって、それが、後でも少しお話ししますが、六つの層を作って、それが非常に複雑な構造を作って初めて機能します。ですから、そこが傷んでくると非常に修復が難しいですし、また実際に光を受ける部分ですから、直接的に失明につながるというふうになります。
高橋:それを作るというのはやっぱり相当難しいことだったんでしょうね。
笹井:そうですね。私たちも、その網膜の中の光を感じる視細胞とか、その神経シグナルを脳に伝えるためのニューロン、それぞれを作るということは、この10年間ぐらいの間に一つひとつ成功してはきてたんですが、六つの細胞がきれいに層を作った構造、こういうものを「組織」と言うのですが、きれいな、機能的な組織が作れるとは初めから期待していたわけではなくて。これができるというのは、一つの夢として思っていた程度だったんです。
高橋:そうすると、その夢をどうやって実現させたのか、CMの後に詳しく伺いたいと思います。ここでいったんCMです。
(CM)
高橋:「科学朝日」、本日のゲストはこの方、理化学研究所発生・再生科学総合研究センターの笹井芳樹さんです。あらためまして、よろしくお願いいたします。
笹井:よろしくお願いいたします。
高橋:まず、再生医療というのが昨今大変注目されているわけですけれども、笹井さんが所属されている発生・再生科学総合センター、ここはまさに生物発生と体の形成・維持のメカニズムを研究し、その応用として再生医療を目指しているというところなんですね?
笹井:はい、そのとおりです。
高橋:これはいつできたんでしたっけ。
笹井:これは2002年に神戸で、大きな形でスタートした、国のプロジェクトとしてスタートしたものになります。
高橋:先日、神戸のポートアイランドに行きまして、研究室にお邪魔しましたんですけれども、理研だけでなくて、さまざまな研究所や医療機関が集まっていて、一大拠点となっているんですね。
笹井:そうですね。実は、神戸は17年前に震災がありまして、その、ある意味復興の一つとして、医療産業あるいはライフサイエンスを基盤にした研究開発の拠点化というのを目指していたんです。そのなかの一つの、国の施策の中に位置づけられています。ですから、作るのであれば世界一の研究所をここで作ろうという意気込みで、みんなが集まってきて、作ったような研究所になります。
高橋:関西の大学との連携もいろいろされているんですよね。
笹井:そうですね。関西だけではなくて、国内のいろいろな形で、ナショナルセンター的な役割もしていますし、国際的な連携もたくさん、いろいろな形でしています。
高橋:すぐ近くに、この間世界一になって有名になったスパコンの「京」があるんですね。
笹井:そうです。神戸の医療産業都市構想というのは、最初は再生医学とか、薬の開発とか、そういった、いわゆる今まであったような生物や医学の最先端を目指していこうというものだったのですが、今回スパコンの京、世界一にめでたくなったわけですけども、これはいろいろなものにも使われます。例えば、宇宙であるとか、海洋であるとか、あるいは震災のシミュレーションとか。ですが、ある意味一番難しいのが、非常に複雑な私たちの体、あるいは細胞などのシミュレーションをしようというもので、それをこのスパコンの京であれば、かなり違った面白いレベルまで分かってくるんじゃないかと期待しています。
高橋:すぐお隣に立っていたので、これで生命科学も、コンピューターを使った生命科学というのが一気に進むのではないかという印象も持ちました。
笹井:私たちも期待しています。
高橋:じゃあいよいよ人工網膜、人工網膜と言っていいのでしょうか、網膜を人工的に作った、それはどういうものなのかをご解説いただきたいと思うのですけれども。CGがあるんですね?

笹井:はい。
高橋:これ、何ですか。
笹井:これはES細胞の培養の仕方です。これは小さなくぼみのある培養皿なんですが、この培養皿の中にES細胞を3,000個バラバラにして入れます。そういたしますと、これが重力によって下に落ちていきますね。きれいに3,000個の細胞が集まって、肉団子のようなお団子を作ります。それを脳に分化しやすい状況に作ってやります。網膜は脳の中からできてきますので、その培養条件を作ってやると、このように網膜になる部分が飛び出してきます。
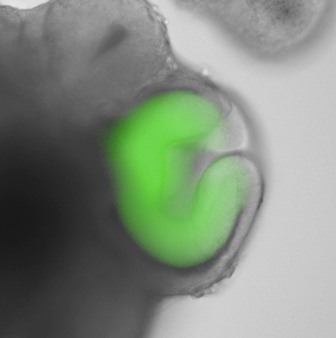
この緑の部分が網膜になる部分です。それだけではなくて、網膜の形である、ブランデーカップのような形が自然とできてくるということを私たちは見つけました。しかも、ここの中には網膜だけがきれいにできていまして、それを切り取って培養してやると、どんどんどんどんこれを大きくすることができます。これで大きく育った網膜なんですが、驚いたことに、網膜の非常に複雑な構造、6種類の細胞が層を成している構造がこの組織の中で見ることができたので、これを今後医療応用、特に再生医療応用に使えないかということで研究をしているところです。
高橋:あの球の形をしている円周の部分が、全部網膜の組織になっているということですか。
笹井:ではなくて、この場合は網膜というところが、脳の間脳というところから発生しますので、その間脳のところをまず作ってやって。そうするとその中に網膜が生えてくる。ですから、あの中の一部が網膜になる、というふうなかたちになります。
高橋:間脳を作ってやるというのは、培養液に何か、それにふさわしいものを入れるということなんですか。
笹井:そうですね。間脳というのは大脳のすぐ下にある部分なのですけども。この絵では、この灰色の部分、ちょっと白っぽい部分が間脳になります。間脳の中から私たちの網膜は発生してきますので、間脳を作ってやると、そこから飛び出すように網膜ができてきたということ。
高橋:間脳から網膜を作るときは、また何か操作をするんですか。
笹井:はい。これは面白いことなんですけども、この間脳自体はES細胞を培養してやったときに、二つぐらいの条件を満たしてやると、わりと簡単に作ることができるということが私たちの研究から分かりました。一つは、培養するときに余計な因子、特に培養するときには細胞がよく増えるように、血清であるとか、増殖因子と呼ばれるようなたんぱく質を入れることが多いのですが、これらを入れてやらないということがまず大事なことでした。つまり、ES細胞が分化するときに、「あなたたちが分化しやすい、自分たちがなりたいものになりなさい」というふうにさせます。そうすると実はES細胞は、「それならボクは、大脳や間脳という、脳の中でももっとも前のほうにある組織になろう」とします。
高橋:へーえ。
笹井:そこで次に、網膜を作るときには、網膜という組織は細胞の外側にある基底膜という膜で覆われているのですが、その基底膜というのがきちんとできないと網膜は作りにくいということが分かっています。そこで基底膜を作るためのたんぱくをこの培養液の中に、まあ材料として入れてやる。そうするとこの細胞たちは、「おっ、これで網膜作れるな」といって勝手に作ってしまったということになります。私たちが特に、ここに眼を作れとか、こんな形で網膜を作れ、というふうなことを言っているのではなくて、この細胞の塊が自分たちの中で、いわば話し合って、「よし、ボクらは好きなものになれと言われてるんだから、間脳のあたりの神経になろう」と。それで、しかも網膜になれる材料がある。「じゃあ自分たちは網膜になろう」というのを、どうも勝手に話し合って決めていたというのが。
高橋:そうなんですか(笑)。
笹井:研究した結論としてはそういうことになります。
高橋:ちょっと一つひとつ、もうちょっと詳しく伺っていきたいのですが。今まで何度も出てきたES細胞という言葉ですね。皆さんもお聞きになったことはあると思うんですけども、「でも、それ何」って聞かれると、よく分からないと思うので、まず、ES細胞とは何かというところからご解説いただけますでしょうか。
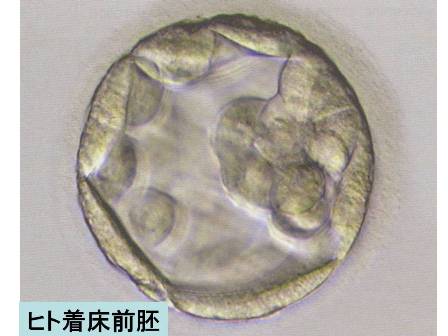
笹井:はい。そうですね、私たち、まあ、ほ乳類ですね、の体は、すべて卵子と精子がくっついて、受精卵となって、それが2個、4個、8個と分裂していって、胎内で着床をして、赤ちゃん、胚に発生していきます。この過程の中でこの胚は、非常にいろいろな、例えば神経があったり、心臓があったり、腎臓があったり、いろいろなものを持っているのですが、その一番最初の段階では、細胞たちはどんな細胞にでも変わることができる、そういった能力を持っています。それが着床する寸前の胚の中にありまして、それを取り出してきて、試験管の中で無限に増えるようにした、そういったものをES細胞と言います。これは、少し前に、4年ほど前でしょうか、ノーベル医学・生理学賞が、このES細胞の発見ということで、マーティン・エヴァンズ先生に授与されたことでも記憶に新しいと思います。
高橋:ええ。で、必ず出てくるのがiPS細胞という言葉ですね。
笹井:そうですね。
高橋:iPS細胞とES細胞の違いというのはどういうことになりますか。
笹井:このES細胞は、いま申しましたように、着床する寸前の胚の、この部分が赤ちゃんになる部分なんですが、このところから作ったものなんです。これと同じ性質を持ったものを私たちの体の細胞、例えば皮膚の細胞などに、遺伝子操作をして作り出したもの、これがiPS細胞です。ご存知のように、京都大学の山中(伸弥)先生が発見されて。これは非常に私たちにとっても画期的なもので、私たちもES細胞とこのiPS細胞は両方とも平行していろんな研究に使うようにしています。
高橋:作り方は違うけれども、性質としてはES細胞とiPS細胞は同じと考えてよろしいんですね。
笹井:そうですね。これは、できた元は違いますけど、いったんできてしまうと、私たち実際使っている研究者でもどっちがどっちか区別がつかない。
高橋:あっ、そうなんですか。
笹井:培養細胞を培養皿の中に入れていて、ちゃんと僕らはもちろん印もしますし、実際には違う培養の孵卵器の中に入れるんですけども、そうじゃなくてゴチャゴチャにしてしまったら分からなくなるぐらい、よく似ています。
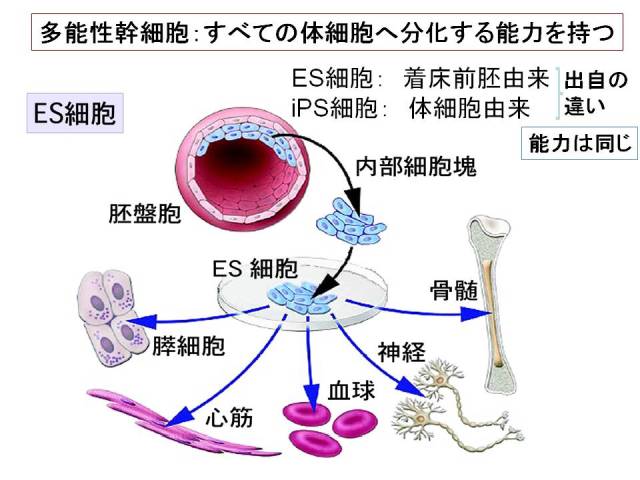
高橋:ああ、そうなんですか。これは、さっきご説明いただいたように、いろんな細胞になりうるってところが一番の特徴なわけなんですね?
笹井:そうですね。このES細胞という細胞は、試験管の中で培養してやるとさまざまな細胞に変わっていくことができる。こういった非常に未熟な細胞から私たちの体を作っているような成熟した細胞を作っていくことを「分化をさせる」と言いますが、ES細胞はさまざまな細胞に分化することができます。さらにこのES細胞を胚の中に戻してやると、胚の中ですべての体の細胞に分化することも証明されています。それが、「ノックアウトマウス」という遺伝子破壊をする技術があるんですが、そういう大事な技術につながっています。これも4年前のノーベル賞の一部になりました。ES細胞は試験管の中でさまざまな細胞に分化する能力を持っているんですが、これは、ただ培養だけをしていると、普通はランダムにさまざまな細胞に変わって、特定の欲しいものだけに変わるわけではありません。どうしてやると神経なら神経、網膜なら網膜だけに分化させることができるのか。選択的に分化をさせる、そういった技術をこの10年間多くの研究者が研究してきていて、その研究の成果の延長線上に今回のお話もあります。
高橋:なるほど。じゃあ普段ただ培養していただけだと、何になるかは、人間のほうには分からないわけなんですね?
笹井:そうですね。通常の、よくES細胞を普通に培養する方法で、ただ分化を多少しやすいような工夫をしてやる程度であれば、いろんなものが混ざって出てきます。
高橋:へえ。そのなかで、さっきご説明のあった、間脳にするというやり方はもう確立されていたということなんですね?
笹井:そうですね。このときには通常の培養と違って、例えば血清を入れないとか、増殖因子を入れないとかいう、少し、「あれ、いつもと違うな」ということで、ES細胞は、そうなると実は間脳のほうにすっと持っていくことができるということが、まあ私たちの研究で、ある偶然で見つかったのです。それができてから非常にこの脳の研究は進むようになりました。
高橋:なるほど。今回は目標が網膜ということでしたので、網膜についても簡単にご説明いただきたいと思います。
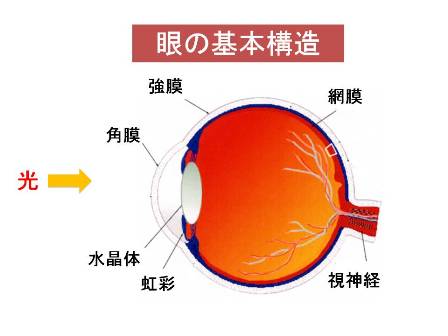
笹井:網膜は、私のたちの目の中で一番、ある意味重要な機能をする部分です。網膜は、カメラでいうとCCDにあたるところで、光を受けて、それを電気信号に換えて、それを脳のほうに伝えていく、その三つの機能を持っています。網膜は、光を受ける視細胞と、それを信号に換えるいくつかの神経細胞、そしてその神経細胞が最後は脳につなげるための神経繊維を伸ばしていく。一口で言うと簡単なんですが、実はちょっとビックリするぐらい複雑なネットワークを作っています。私たちは、この複雑な部分、神経網膜をES細胞から今回は作るようにしたんですが。実は冒頭にありました、色素上皮という、これを保護するような細胞に関してはもう数年前にES細胞からきれいに作ることができるようになっていました。今はそれを病気の治療に用いるぐらいのレベルまで進んでいるわけです。
高橋:日本でもその研究が進んでいるわけですね、アメリカだけではなくて。
笹井:そうですね。私たちの神戸の研究所では、世界の非常に最先端のしのぎを削るような研究がなされています。ただ、こちらの神経網膜のほうは、これまで1個1個のパーツは作れてもこうした複雑な構造を作るということができなかったので、これを治療するということに関してはまだなかなか難しいかなという状態であったわけです。
高橋:1個1個のパーツを作るときは、間脳を経ないで作っていたわけですか。
笹井:そのときには、間脳を作ってはいるんですけども、今回のように立体的に作るのではなくて、培養皿の中にペタッと貼り付けて作っていた。細胞はバラバラにいろんなものになるんですけども、2次元の世界なので、こういう構造を作ることができなかった。で、今回の私たちの方法の一つの特徴は、3次元でES細胞を培養して。ですから立体的な構造を作りやすい状況で、「あなたたち細胞が作りたいものは何ですか?」と言ったら、実はちゃんとした構造を作ってしまったということになります。
高橋:3次元というのは、先ほど、最初のCGに出てきたような、フラスコじゃないですね(笑)、試験管、ほんとに小さな試験管の中に入れてやるということなんですね。
笹井:そうですね。ES細胞の塊を、ボールのような形で培養液の中で浮かしているというふうなことになります。
高橋:自然に浮いちゃうわけですね。下まで、底につかないんですね?
笹井:基本的には下まで行くんですけども、下に着いたり、浮いたり、着いたり浮いたりみたいな感じです。
高橋:そうなんですね。これはCGでしたけども、実際に細胞が変わっていく姿を顕微鏡で撮っていらっしゃるんですね。
笹井:そうですね。
高橋:じゃあそれも出ますでしょうか。
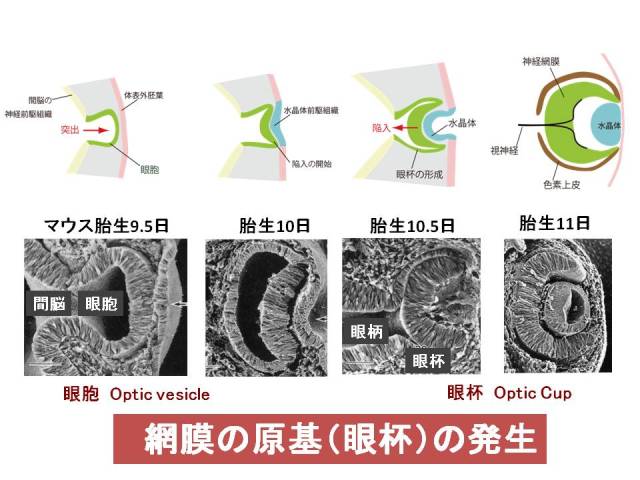
笹井:今からお見せしますのは、ES細胞の培養をしたときに、ちょうど胚の中で、これはマウスの赤ちゃんの非常に早いうち、妊娠の早いうちの赤ちゃんの網膜がどうやって発生するかを示しているものなんですが、ここで見られた現象が試験管の中でも再現することができたというお話です。先ほどから出ております、間脳という部分が飛び出してきて、袋のような形、「眼胞」というものを作ります。これが網膜の元になるのですが。網膜はこういった袋ではなくて、この先の部分がどんどん折れ曲がっていって、このブランデーカップを二重底にしたような形、「眼杯」という構造を作ります。これが、あとどんどん大きくなって私たちの網膜になるわけです。ですからこの眼杯というのができるということが、赤ちゃんの網膜ができたということと同じ意味なんですが、これがES細胞の培養系で立体的にできるようになったということをお示ししたいと思います。
高橋:はい。じゃあビデオが出ますでしょうか。
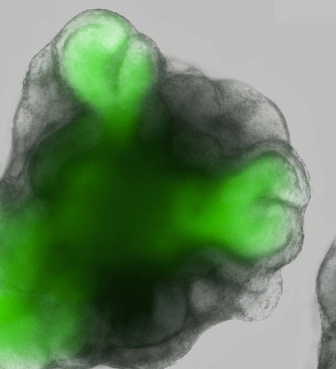
笹井:これはES細胞を固めて3日目からのビデオなんですが、グリーンで光っている部分が網膜になった部分です。これは、下村(脩)先生の見つけられたGFPというものを使って見えるようにしています。さらにこの培養を続けるとこのブランデーカップのような構造を作ります。ここはもう一度別の角度から見ていただくのですが、ここでこのカップのような構造ができていることが分かります。これは3次元なのでなかなか分かりにくいと思いますが、3次元再構成したものをお見せいたします。これは断面をお見せしているのですが、はじめ袋状だったものがへっこんで、ブランデーカップのような構造ができていることが分かります。ここでとても大事なのは、これはES細胞の大きな塊から飛び出してきて、へっこんでいったという過程をお見せしたんですが、この周りに何もほかの細胞はありません。ですから、袋状に飛び出した網膜が、こうやってブランデーカップのような構造を作っていくときに、例えば外から押されてへっこんだわけでもなく、何かで形を成形するようなことでできたのでもなくて、どうもこの網膜の細胞たち、これはシート状の構造を作っているのですが、そのシート状の構造が勝手に自分で変形してこの形を作ったということがわかります。実はこれは僕らにとって非常に大きな驚きといいますか、ビックリしたことで。こんな複雑な構造を、実は細胞の集団、ここは1,000個程度の細胞が最初あったと思うんですが、それらの細胞たちが勝手に自分たちで作ってしまう。どういう形を作ったらいいのかを彼らは実は知っている。ここに非常に大きな、生物らしい不思議さを感じました。
高橋:近くの細胞から何か指令を受けているんじゃないかという考え方もありましたよね。
笹井:そうですね。これは、実は発生学のなかで100年ほど前から、ハンス・シュペーマンというノーベル賞をもらった有名な発生学者がいるんですが、その人の時代からずっと、どうしてこんな形ができるんだろうかということは議論の的で。ある人は、すぐ近くにできる水晶体(レンズ)が押してるんじゃないかとか、その周りの角膜が形を決めてるんじゃないか、などといろいろな説明があったのですが、実はそうじゃなくて網膜自身が、自分がどうなるべきかをちゃんと知っている、と。私たちが余計なことをしないで、「なりたいものになりなさい」と言ったら、彼ら(細胞たち)はこういう形を作ってしまうということで。とても生物は奥が深いといいますか、細胞たちは僕らが思っているよりもずっと賢いということを感じました。
高橋:それは、すべての細胞がそうなんですかね。網膜細胞はそうだけれども、ほかの細胞は、例えば網膜からの何か指令を受けて変わっていくとか。
笹井:そうですね。体の中にはさまざまな器官がありますので、その器官を作っていくときに、ほかの部分が「おまえ、こういうふうなものになれ」というのを指令している場合があることも知られています。
高橋:あっ、それは実際にあるんですね。
笹井:はい。ただ、実は細かいところは、それでも自分たち、組織の中で結構プログラムされている。ややこしい言い方をすると「内的なプログラム」といいますか、自分たちの中が持っているプログラムというのが結構決めていて、実は外から言われている指令というのは、意外と細かいことでなくて、大ざっぱな指令、「キュー」さえ入れれば後は作ってしまうのではないかという、新しい発生の原理が少し今見えてきたように思っています。
高橋:それにしてもちょっと複雑な形ですね、眼杯と言われている、そういう複雑な形を。それぞれは同じ種類の細胞なんですよね。なんでこういう形ができてくるのか不思議ですよね。
笹井:そうですね。実はこの眼杯というのは、最初に三つの、似てるけどもちょっと違う細胞になります。一番外側の薄い部分が、後で色素上皮に変わるところです。この中側の分厚いところ、今ここは緑で光らせるようにしている部分ですが、ここは神経網膜、光を受ける視細胞などを作るところです。その継ぎ目のところがまたちょっと違う細胞がありまして、この三つの細胞がまず、もともとは同じ細胞からだったのですが、分かれていって、どうもこの間でお互いにやりとりをして、「じゃあオレはここでちょっと曲がろう」とか、「オレはここで大きくなろう」とか、「薄くなろう」とかいうことを、どうもお互いの話し合い、まあ生物の言葉で言うと「組織と組織の間の相互作用」でそれを決めているということが分かってきました。
高橋:その3種類あれば、形はわりと自然にこういうふうになるということなんですね。
笹井:そうですね。ただ、そういうことがそんなに、何と言うのでしょうか、すぐは信じられないようなことだったんですね。
高橋:そうですね、ええ(笑)。
笹井:それが信じられるようだったら100年間も議論はしてなかったわけなので(笑)。ですからこれは、とは言いながら、なんかこの辺のほかのものが変な力を入れてて、思わない、知らないような何かがかかっているんじゃないかということも思ったのですが、そうした研究をしていくときに、これらの細胞がどんな挙動をするかというのを、培養の間ずっと今顕微鏡で見ることができます。先ほども3次元構成したものをお見せしましたが、あの中で、実は1個1個の細胞がどんな形になるとか、いつどんなふうに分裂するかも全部、今、調べることができます。そうした定量的なデータを基にそれをコンピューターの中に再現してやると、じゃあそのことでこんな形ができるのだろうか、というのを調べることができます。
高橋:それは力学的なシミュレーションということになるわけですね。
笹井:そうですね。先ほども神戸の京の話がありましたが、今、ライフサイエンス、こうした生物学と計算科学や数理科学をドッキングさせて、より深い生物の理解や新しい制御法を見つけていこうという研究を、私たちの神戸の理化学研究所でも盛んにしているのですが、こうした顕微鏡でのデータを「シミュレーション」と言いますが、計算機の中で再現してやると、実はこういった形ができるというのもお見せできると思います。
高橋:はい。では、シミュレーションが出てきますでしょうか。これですね。
笹井:これは、そうしたデータを入れてみたものです。まずこの緑の部分が少しやわらかくなります。そのうえで継ぎ目が変形して、次に緑の部分が大きく増殖すると、実はこういった形ができる。これは、コンピューターグラフィックスでやっているのではなくて、そうしたデータを入れて、計算式を入れて、あとコンピューターに「勝手に計算しろ」といったら、実はこういったものができたので。これはどうも主観的なものではなくて、ほんとにこういうことが起きうるんだということを示しています。ですから、どうも外から何かの力がなくても、内部の力学的な性格が、順番を追って変わっていったり、増殖があるところで速くなったりするというような、生物学的に可能な原理を基に、こうした形はなかのプログラムで決まっているんだ、ということがこれで確認されました。
高橋:じゃあ、形はこういうふうにできるんだということは分かりました。だけど、その網膜の6種類ですか、の細胞がきちんと層状に並んで出てくるというのは、これはまた不思議なことなんですけど。
笹井:そうですね。こうした複雑な構造が、なにもバームクーヘンを作るように、お腹の赤ちゃんの中で誰かが付けてるわけではないわけですね。これも細胞たちが、ある意味相互作用をして、話し合って、「こういった形を作ろう」ということなんだろうというのは想像できるんですが、実際そうなのかというのを確認する術というのがなかなかなかったんですね。今回、わりと単純なES細胞の培養系でこの過程をすべて見ることができましたので、実際それが起きているということが分かりました。ここにある6種類の細胞が層を作るのですが、ES細胞を培養していて10日ぐらいで先ほどのカップのような構造ができます。
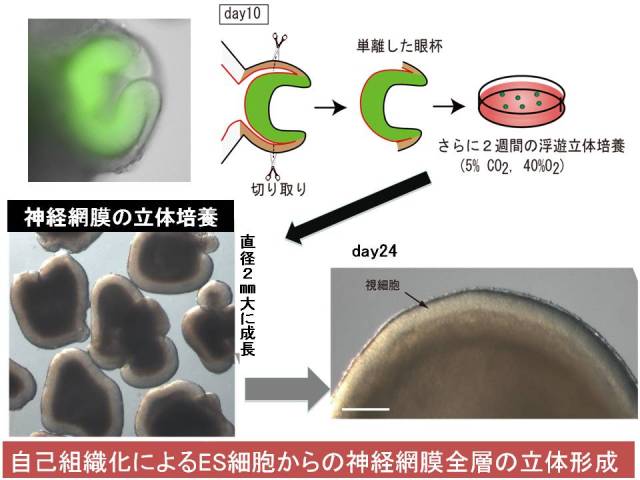
高橋:ブーッとふくらんでくる。
笹井:はい。それをさらに培養を続けると、自然とこの層構造ができることを見つけました。これが10日たったところのカップの形なんですが、それを切り出しまして。そうするとこれは純粋な網膜になっています。これをやはり浮かした形で立体的培養、2週間続けてやりますと、この網膜の部分はどんどんどんどん大きくなって、初めは0.2ミリぐらいの直径のものが、2ミリ。10倍に直径がなるというのは、体積で言うと1,000倍になっているので、非常に大きくなっています。これはマウスのES細胞からしたのですが、マウスの新生児の眼ぐらいの大きさになってしまっているわけですけども。それを調べてみると、非常に均一なきれいな形で、整った細胞のシートになっていて、しかも裸眼で見てもいくつかの層ができているということが分かります。
高橋:そうですね。これは中空なんですか?なかは空っぽ?
笹井:はい。この中は空っぽになります。これを顕微鏡で調べてみると、先ほどお示しした六つの細胞がきれいに層を作っていて、しかもその間にシナプスと呼ばれる、信号を伝える構造もできていたということが分かりました。ですから、ES細胞が作った網膜は、ただ網膜の元ができただけではなくて、生まれた後の網膜の形を作るプログラムもちゃんと持っている組織ができていたということが分かりました。
高橋:じゃあこの方法で、ゆくゆくは人の網膜も大量生産ができるということになりますね。
笹井:そうですね。今、私たちが神戸の研究所で力を入れていますのは、まず眼杯という、胎児の、赤ちゃんの網膜になるものですが、これをES細胞、ヒトのES細胞、あるいはヒトのiPS細胞を使って作って、それをさらに大きくして、六つの層ができるような網膜ができるだろうかと。その研究に非常に力を入れて、なんとか近いうちに、それは10年とかいう先ではなくて、1年とか2年とかいう単位で現実的にそうした組織を作りたいと思っています。
高橋:ただ、移植するとなると、やはり拒絶反応というのが常に問題になるのですけれども、網膜といえどもやっぱり拒絶反応というのは起こりえますよね。
笹井:そうですね。私たちの体は、他人の組織が入ってくるとそれをはじくような拒絶が起こるわけなんですが、どういった細胞を移植されるかによって実はかなり拒絶の力が違います。そのなかでこの網膜というものは、脳と同じような性質を持っていまして。脳や網膜の細胞は、比較的、他人の体の中に移植しても拒絶が少ないという性質を持っています。ですから私たちは、これは移植をして、少しは免疫を弱くするような薬を一時的には使う必要があるかもしれないんですが、たぶん非常に弱いお薬程度で移植は成功するのではないかと期待しています。
高橋:なるほど。そういう点からも非常に期待が高まっているということなんですね。
笹井:はい。現実的な治療法につながりうる可能性が高いと思っています。
高橋:なるほど、分かりました。いったんここでコマーシャル入れます。CMです。
(CM)
高橋:「科学朝日」、本日は理化学研究所発生・再生科学総合研究センターの笹井芳樹さんをお迎えしています。さて、これまで網膜を作り出す研究についてお話を伺ってきましたけれども、網膜以外のものも作っていらっしゃるんですよね。
笹井:そうですね。私たちの研究所では、発生という、一つの受精卵から体のさまざまな組織がどうやってできてくるのか……。ある意味とても不思議だと思うんです。ただ単に分裂しているだけでは、肉団子がどんどん大きくなるだけのはずなのに、なぜいろいろな組織ができてくるのか。
高橋:そこが一番不思議なんですよ、生物の。
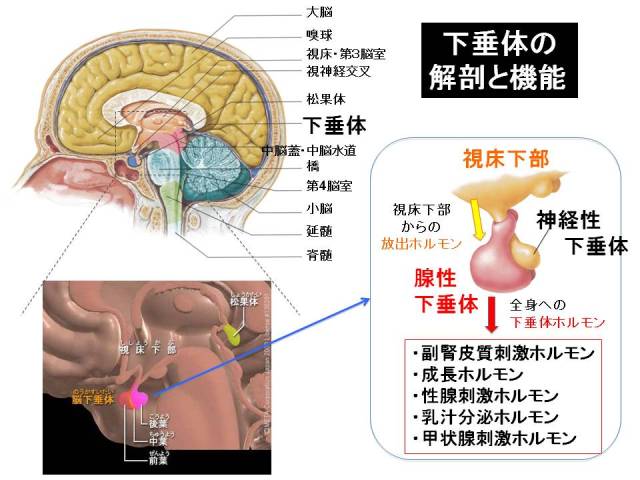
笹井:そうですね。それが研究所の中心的な研究なので。一つの網膜ができるだけではなくて、それがほかの過程ではどうして違うものができてくるのかという研究もしています。そのなかで私たちの研究室では、網膜以外にも大脳がどうやってできるかとか、小脳がどうやってできるかとかも研究しているんですが、一番最近面白い成果として出てきたものが、「下垂体」と呼ばれる、内分泌の臓器がどうやってできるのか。それについてもこのES細胞などの分化系を使うことができるということが新しいものとなっています。
高橋:下垂体というのは、脳の中の、垂れ下がっているものということですよね、下垂というのは。
笹井:そうですね。
高橋:どのへんにあるんでしたっけ。
笹井:この大きな部分、黄色い部分が大脳でありますけれども、その下に間脳、ピンクの部分がありまして、そこからぶら下がっている、懸垂しているものが下垂体ということです。この下垂体自体は、実は脳の一部ではなくて、脳じゃない組織が脳にぶら下がっているという意味でこういうふうな名前がついているのですけれども。
高橋:ああ、そうなんですか。
笹井:実はどういった機能をしているかというと、これが体のホルモンを司る司令塔みたいな、コントロールタワーみたいな役割をしています。これは、脳の視床下部というところから、全身の恒常性、体の状態をこういうふうに制御しなさいという指令を受けて、それを基に体中にさまざまなホルモンを分泌していきます。特にこの副腎皮質刺激ホルモンというものは非常に重要で、これがないと私たち人間は3日もしないうちに命の危機になるというような重要なホルモンですし、ほかにも体を成長させる成長ホルモンや、また私たちの体の中でも性を、男性は男性らしく、女性は女性らしくするようなことを司っている性腺刺激ホルモンなど重要なホルモンを出しています。
高橋:女性の体のリズムを作り出すのも、ここだということですね。
笹井:そうですね。これが傷むと、そうした、月経なども止まってしまうということになります。
高橋:成長ホルモンも、子ども時代にこれが欠けると大きくならないという病気がございますよね。
笹井:そうですね。そうしたときにこうしたホルモンの補充療法も一部されているのですが、それでなかなかうまく治療できない場合も多いわけです。
高橋:下垂体を再生科学で作り出すことができれば、こういうホルモンが欠けるという病気の方に非常な朗報になる、こういうことですね。
笹井:そうですね。ただ、実はこうした内分泌ホルモンを作るような器官というのは、研究がなかなか進んでいなかったところがあります。特にこの下垂体は複雑な発生の仕方をします。それで研究が進みにくかったこともあるんですが。そうしたスライドが、たぶん次に用意されていると思うんですが。
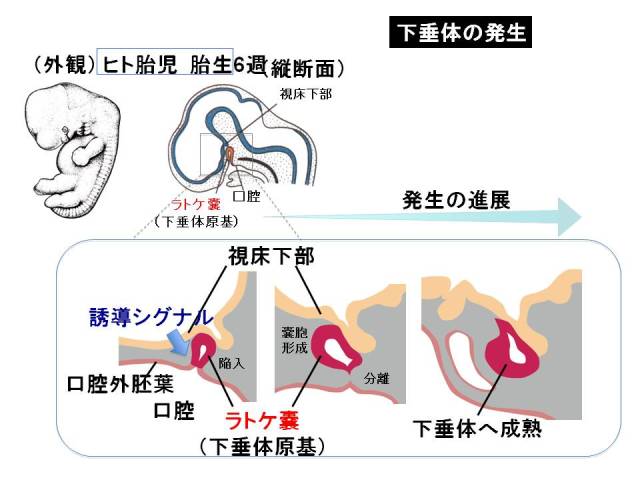
この下垂体は、ヒトの胎児でも、妊娠して非常に初期の時期ですね、の頭のところでできてくるんですが。実は私たちの口の中の粘膜、上あごの粘膜に脳からの何らかの刺激が来て、そのせいでこの部分が下垂体に変わって、大きくなってぶら下がるというふうになっています。非常に複雑な発生をして、しかも非常に小さな臓器として初めはスタートしますので、この研究はなかなか解析が難しかったのですが、今回は、先ほど網膜の培養をするときに使ったこの浮遊培養法、それを工夫して。網膜の場合、それが非常にきれいな形で眼杯を作りましたね。
高橋:ええ、作りましたね。
笹井:あれとはまた少し違う、いくつかの、培養液に入れるものとか、培養条件を使うのですが、そうすると実はここ(下垂体発生)の環境そのものを再現することができるようになりました。そうすると、網膜のときには自分で勝手に眼杯を作るということをしました。こういうことを「自己組織化」と言うのですが、実はこの下垂体の元になるラトケ嚢と呼ばれる構造が、やはり同じように勝手にES細胞の塊の中にできてくるようになりました。
高橋:ほお。この袋みたいな形ができてくるわけですね。
笹井:そうですね。
高橋:この袋の形だけじゃなくて、「ホルモンを出せ」という指令を出すという、その機能の部分はどうなんですか。
笹井:このラトケ嚢という下垂体の元になる部分は、12日ぐらいでできるんですけども、それをさらに2週間ぐらい培養してやると、その中にたくさんホルモンができてきまして、それを刺激するとたくさんのホルモンを培養液の中に放出するということを見ることができました。
高橋:じゃあちゃんと下垂体として機能するものができたということなんですね。
笹井:そうですね。非常に私たちの体の下垂体とよく似たものができていたので、それを本当に私たちが、体の中でホルモンをコントロールしているぐらいの機能まであるのかというのを調べるために、移植実験を行いました。
高橋:ほお。それは?
笹井:移植をするときには、下垂体をまずマウスから取ってしまいます。そういたしますと、放っておけば、下垂体がないせいでホルモンがどんどん下がっていって、マウスは非常に活動が落ちてきます。放っておけば死んでしまうことになるわけです。そのかわりにES細胞から作った人工下垂体を体の中に移植してやると、それが助かるかどうか、そういった実験をしてみました。両方ともマウスは下垂体を取ってあるのですが、こちらはES細胞から作った下垂体を移植したもの、こちらは下垂体を移植してないものです。このネズミはハムタローというか(苦笑)、ハムスターと一緒で、こういった回し車が大好きで、乗るんですが、こちらは非常に活発に動くのに対して、こちらはすぐ疲れて、降りてしまいます。
高橋:ほんとだ。この差はもうはっきりしていますね。
笹井:ホルモンがちゃんとある、なしというのは、ものすごく明確に出ます。
高橋:へえ。
笹井:このように、こちらは私たちの、下垂体が傷んだ病気のモデルマウスになるわけですけども、それをこの程度はっきりとしたかたちで治療効果があったということで、これは新しい再生医療の対象として、下垂体などの内分泌疾患も注目されるようになったというふうに考えています。
高橋:じゃあ網膜に続いて下垂体も人工的に作ることができた、と。
笹井:そうですね。
高橋:マウスでできているわけですけれども、ヒトのES細胞で作るというところは難しくないんですか。
笹井:実は、このマウスの研究はつい最近出てきた研究でありまして。今、論文を発表した後にヒトのES細胞、あるいはiPS細胞を使ってこうした研究を行おうと。これを、同じような研究を行ってやはりこのような移植効果があれば、それを次にはより大きな動物で、最終的にはヒト、患者さんの治療に使えないかということを目指すために、内分泌内科の先生方と今いろいろな討論をしながら研究の戦略を練っているところです。
高橋:これからどうやっていくかという戦略を作っている段階ということですね。
笹井:そうですね。というのは、今まではこうした治療ができるということ自体が考えられてなかったんですね。下垂体など手に入れようがなかったので、いわばほんとに新しい治療法の発想になってくるので、こうした戦略を練るのが非常に面白い時期だとも言えると思います。
高橋:再生医療って大変注目されていて、マスコミにも何度も報道されていて。ただ、一方で、期待が先行しすぎるというような声もありましたよね。
笹井:はい。
高橋:実際いまお話を伺っていても、人間に使えるようになるまでにはまだちょっと時間がかかるようですね。
笹井:そうですね。
高橋:ただ、基礎研究でこれだけさまざまな成果が次々出ているというのは、ちょっと私自身も驚きですし、あれですね、日本でがんばっているのは山中先生だけではないということがよく分かりました(笑)。
笹井:もちろん山中先生は大変がんばっていらっしゃいますが(笑)。彼のiPSのような技術というのも、こうしたいろいろなほかの技術と組み合わされて真価を発揮するのだろうと思います。
高橋:特に笹井さんは発生生物学がご専門でいらして、基礎をやってらしたのが、これだけ臨床に直結するようになってきたというところが面白いですよね。
笹井:そうですね。私自身は元は内科医だったんですけども、やはり治せない病気がたくさんある。そういうなかで、私は基礎研究者になって、少なくとも移植する材料はいいものを作ることができるようになってきましたので、これを今度実際動物に移植する、そしてヒトに、ということになると、やはり臨床の外科の先生とか、眼科の先生とか、そうした先生方とのタイアップ、そこにどんどん技術を移転していくということが大事で、そうした活動に力を入れてやっていきたいと思っています。
高橋:それから、あとは何をターゲットにするんですか?下垂体の次に作り出そうとしているものは?企業秘密ですか。
笹井:いや(笑)。いくつか、もちろん狙っているものはあるんですけども、私自身は脳の発生が専門なので、今一番力を入れているのは大脳の皮質、大脳のシワシワの部分ですね、あそこをなんとかきちっとした形で作れないかと。実は数年前に、非常に初期の胎児の大脳の構造を作ることは、やはり網膜と同じようにES細胞からできるということを示しています。ですけども、その胎児の状態から、生まれた後の大脳はもっと複雑になってくるんですね、その過程をまだ完全には再現できてないので、今、一番私たちにとってチャレンジを感じることというのは、ES細胞から作った大脳の皮質の元を、生まれた後の大脳のようにしようと。そのときもやはり6層の層があるんですが、この層をきちっと作ることができれば。これをさすがに移植するかどうかは別にして、例えばアルツハイマー病の研究とか、なかなかヒトを使って研究するのが難しいものが、iPS細胞を使って、患者さんの細胞から作った大脳皮質を作って、そこに薬とか、ワクチンとか、遺伝子治療とか、そういったものを最適化する系として非常に有望ではないかと。これができれば非常にすばらしいなと思っています。
高橋:今後もいろいろな成果を期待したいと思います。ぜひがんばってください。
笹井:ありがとうございます。
高橋:「科学朝日」、本日はこの辺でお別れいたします。次回もどうぞお楽しみに。
有料会員の方はログインページに進み、朝日新聞デジタルのIDとパスワードでログインしてください
一部の記事は有料会員以外の方もログインせずに全文を閲覧できます。
ご利用方法はアーカイブトップでご確認ください
朝日新聞デジタルの言論サイトRe:Ron(リロン)もご覧ください